どのような病気?
フォン・ヴィレブランド病(VWD)は、「フォン・ヴィレブランド因子(VWF)」というタンパク質が生まれつき作られない、もしくは正しく働かないことにより、血が固まりにくくなる、出血性の遺伝性疾患です。
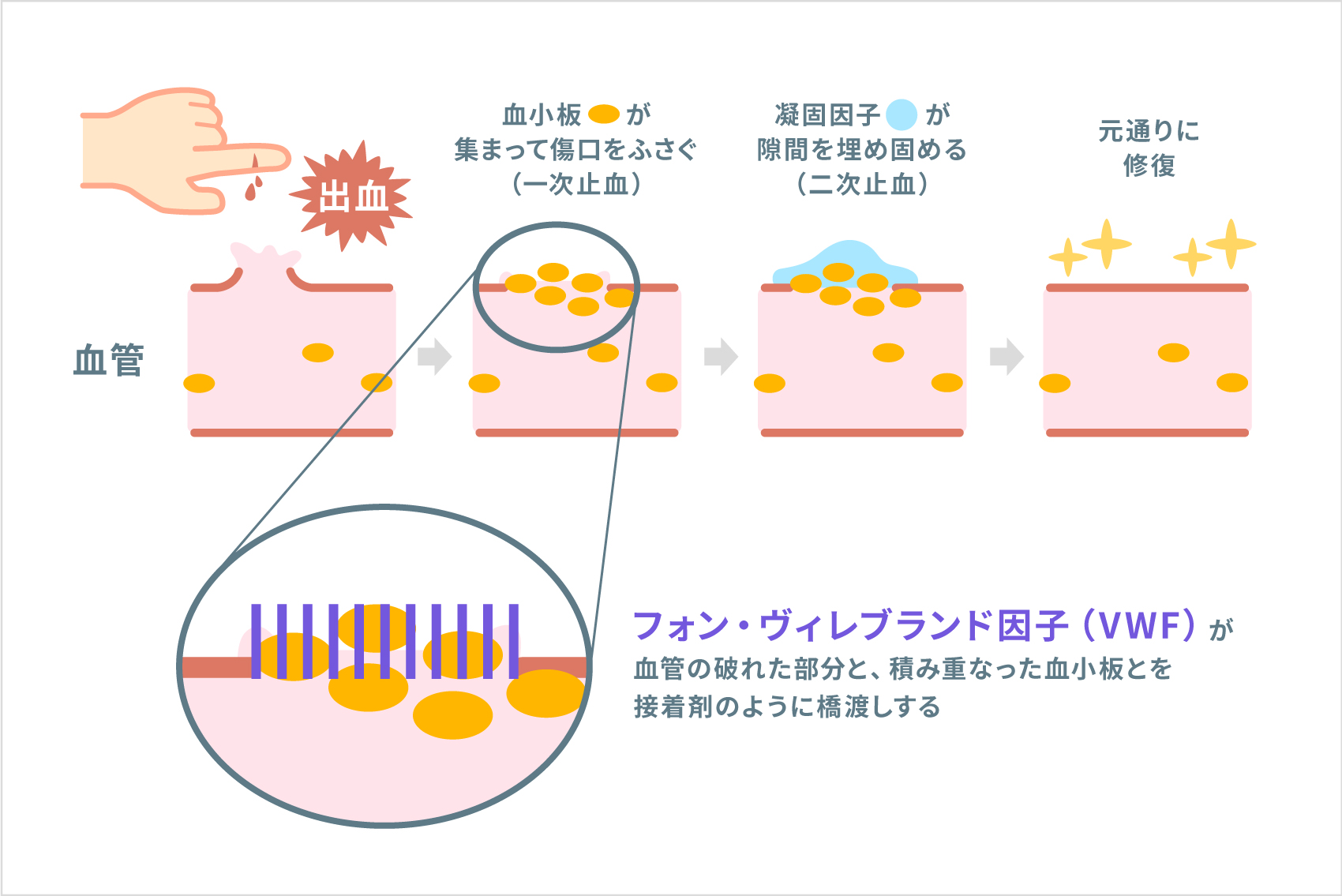
けがなどで血管が破れ出血すると、まず血管の破れた部分をふさぐために、血小板という血液細胞が集まって土のうのように積み重なります。これを、一次止血といいます。次いで、血中に含まれる「凝固因子」と呼ばれるタンパク質が、セメントのように集まった血小板の隙間を埋め固め、止血します。これを、二次止血といいます。
VWFは、血管の内皮細胞などが産生し分泌するタンパク質で、一次止血で重要な役割を果たします。VWFは、お互いにたくさんくっつき合った「多量体」という姿になって、血管の破れた部分と、積み重なった血小板とを、接着剤のように橋渡しするのです。したがって、VWFが正しく働かないこの病気では、一次止血がうまく行われません。また、VWFのもう一つのはたらきとして、二次止血の際に凝固因子の第8因子を、血小板が重なった部分に運んでくる役割もあります。
二次止血の仕組みに病気の原因がある血友病も、同じく出血性の遺伝性疾患ですが、VWDの出血症状は軽度から中等度で、多くの場合、血友病より軽いとされています。また、男性の発症者がほとんどである血友病と異なり、VWDは男女ともに同程度の割合で発症します。
主な症状は、手術や歯の治療後に多く出血して止まりにくい、皮下出血(あざ)ができやすい、鼻血が止まりにくいなどです。軽度のVWDの場合、手術や大きなけがをしたことがきっかけで気付くケースもあります。女性の場合、月経過多や、出産時に多量に出血することもあります。症状が重い人は、けがをしていなくても、あるいはちょっとしたけがでも、出血を起こす場合があります。また、VWDの出血症状は、年齢が高くなったり、妊娠したり、運動をしたり、ストレスがかかったりすることにより、起こりづらくなるとされています。
VWDは、VWF異常のタイプにより大きく1型~3型の3つの病型に分類され、2型はさらに4つのサブタイプに分類されます。1型は3つのタイプの中で最も症状が軽く、VWD患者さん全体の7割程度を占めます。3型は、最も重篤ですが、患者さんは少数です。2型の4つのサブタイプの重症度は、中等度です。
| 病型 | おおよその頻度 | サブタイプ | VWF異常のタイプ | VWFの働き |
|---|---|---|---|---|
| 1型 | 60~70% | - | 量が少ない | 正常 |
| 2型 | 20~30% | 2A型、2B型、2M型、2N型 | 正しく働かない | 血小板凝集機能の低下 |
| 3型 | 5%未満 | - | 全く働かない(ない) | - |
VWDになる頻度は、人種によって報告が異なりますが、日本では、10万人あたり0.56~0.6人という報告があります。ただし、軽症の人は病院で診断されず生涯気付かない可能性もあります。
「自己免疫性後天性凝固因子欠乏症」のひとつとして、難病指定されている(指定難病288)「後天性フォン・ヴィレブランド病」は、名前が良く似ていますが、遺伝性疾患のVWDとは別の病気です。
何の遺伝子が原因となるの?
VWDは、VWFタンパク質の設計図となる「VWF遺伝子」の変異が原因で起こります。VWF遺伝子は、別名「凝固因子VIII VWF遺伝子」「F8VWF遺伝子」とも呼ばれます。この遺伝子の変異により、作られるVWFの量が減ったり、正しく働かない異常なVWFが作られたりするために発症します。1型VWDは、作られるVWFの量が減るような遺伝子変異が原因となっています。2型VWDの4つのサブタイプは、それぞれVWFが正常に働かなくなるような遺伝子変異が原因となっています。3型VWDは、VWFが完全に働かなくなる、もしくは全く作られないような遺伝子変異が原因となっています。
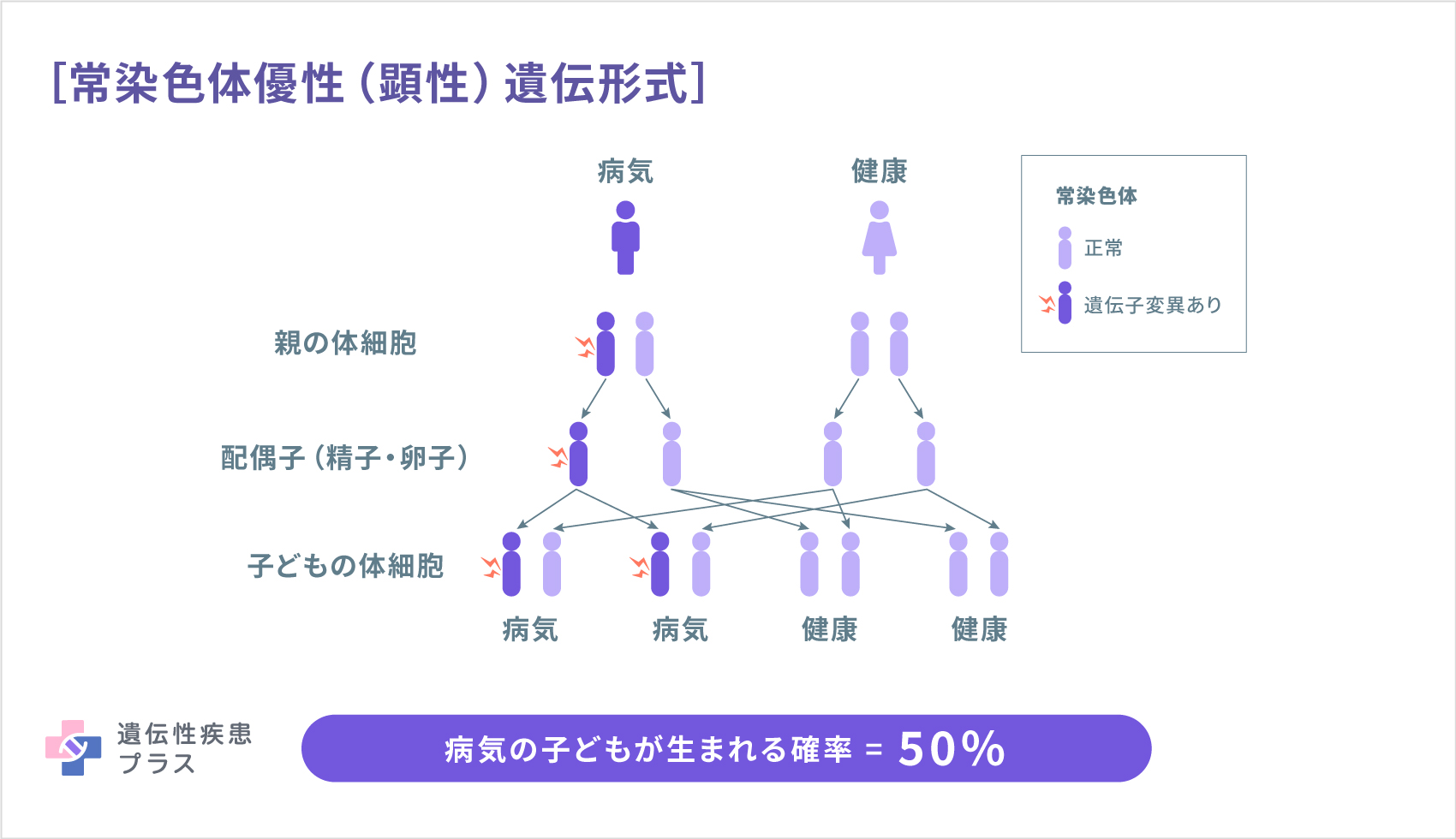
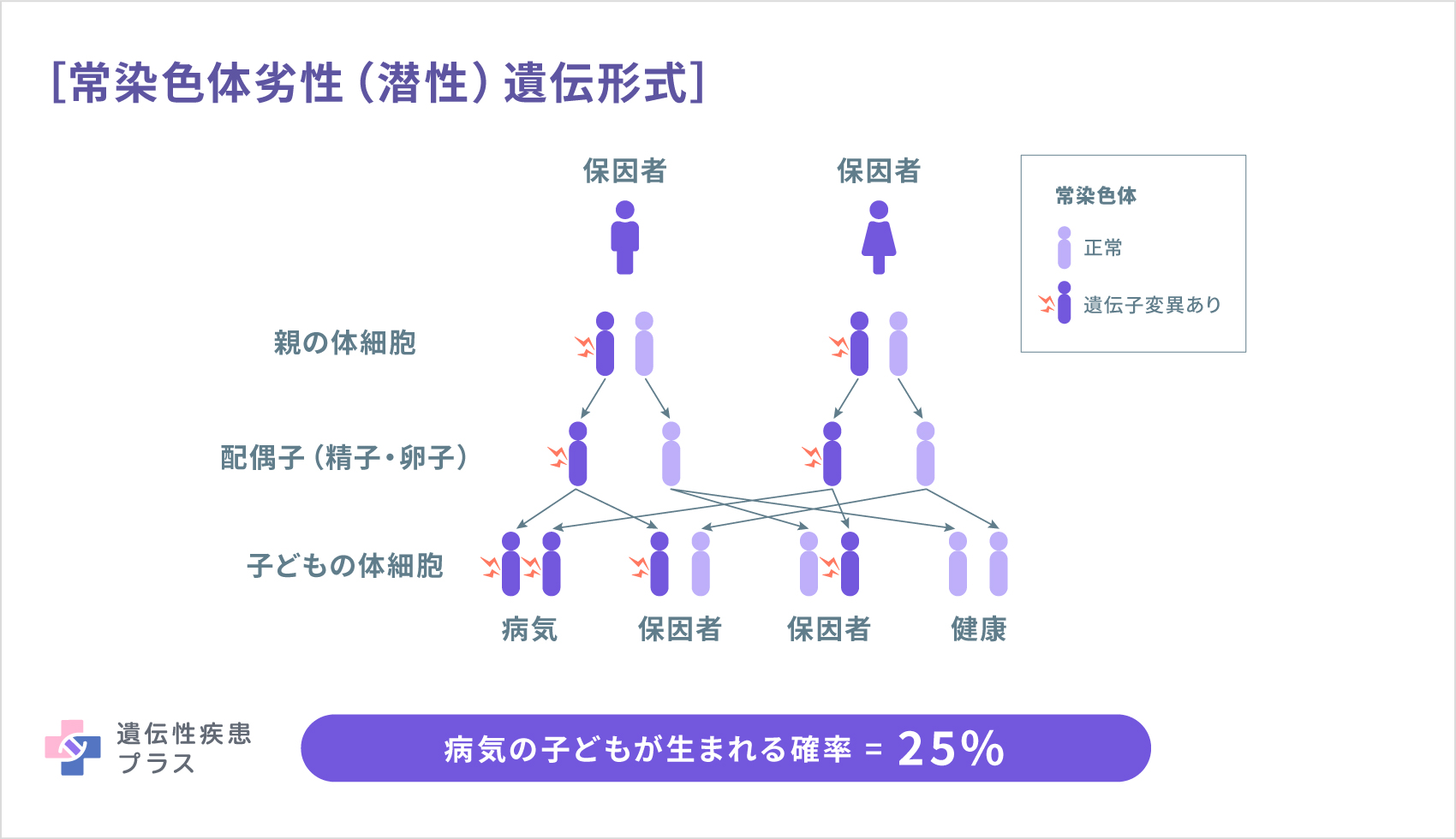
VWF遺伝子は、12番染色体の短腕(12p13.31という位置)に存在します。1型と多くの2型では、常染色体優性(顕性)遺伝と呼ばれる形式で遺伝します。つまり、両親のどちらかがVWDだった場合、子どもがVWDになる確率は50%だといえます。3型と、2型の一部の症例、1型の少数の症例では、常染色体劣性(潜性)遺伝と呼ばれる形式で遺伝します。この場合、人間が2本1セットで持っているVWF遺伝子のうち、両親がともに1本ずつ変異を有していた場合、子どもは4分の1の確率で2本とも変異を有してVWDになります。また、2分の1の確率で1本変異を有し発症はしない「保因者」となり、4分の1の確率でVWDを発症せず保因者でもなく(変異した遺伝子を持たず)生まれます。
どのように診断されるの?
VWDの出血症状や重症度をスコア化する「標準臨床評価ツール」がいくつかあり、これらが診断の一部に使われます。加えて、VWDと診断がつくためには、VWDに特異的な止血因子の検査、または、唯一の原因遺伝子であるVWF遺伝子の分子遺伝学的検査(遺伝子検査)が必要となります。また、ほとんどの場合、診断のために、家系に同じ病気の人がいるかどうか(家族歴の存在)を確認します。一方で、軽症の1型VWDの場合は、遺伝子変異があっても必ずしも発症するとは限らず、これにより家族歴がみられない場合もあるため、診断は容易ではないとされています。
VWDに特異的な止血因子の検査は「機能的VWF検査(VWF:Rco)」「酵素結合免疫吸着検査(VWF:Ag)」「機能的第Ⅷ因子検査」の3つです。これらに異常が認められた場合は、さらに専門的な施設で「VWF多量体分析」「リストセチン誘導血小板凝集(RIPA)検査」「VWFによる第Ⅷ因子結合検査(VWF:FⅧB)」「コラーゲン結合検査(VWF:CB)」が行われます。
こうした検査の数値や、遺伝子検査の結果をもとに、VWDとその病型の診断がつきます。軽症の血友病Aは2N型VWDと類似しており、「VWF:FⅧB」検査はこの両疾患の鑑別に用いられます。この検査の有効性は限られている場合がありますが、分子遺伝学的検査でこの両疾患の鑑別がつきます。
どのような治療が行われるの?
主な治療法は「デスモプレシンによる治療」「VWFを含んだ血液凝固第Ⅷ因子の補充療法」、そして2020年3月に日本でも承認された「組換えVWFの補充療法」です。
デスモプレシンによる治療
デスモプレシン(デスモプレシン酢酸塩水和物、DDAVP、1-desamino-8-D-arginine vasopressin)は、細胞がVWFを分泌するのを促進させる薬です。静脈内注射、皮下注射、経鼻投与などで使用されます。デスモプレシンは、急性の出血症状や手術時に止血をするための治療選択となり、1型VWDの女性患者さんの出産時の出血にも有効とされています。一方、2B型では血小板減少症を悪化させることがあるため禁忌となっています。動脈系疾患を持つ患者さんや70歳以上の患者さんでも禁忌となっています。デスモプレシンは、発作や昏睡を起こす「低ナトリウム血症」を引き起こす可能性があります。そのリスクを抑えるため、デスモプレシンを投与されて24時間以内には、水分摂取が制限されます。
VWFを含んだ血液凝固第Ⅷ因子の補充療法
デスモプレシンによる効果が見られない患者さんや、デスモプレシンが禁忌の患者さんに対しては、VWFおよび第Ⅷ因子を含む血漿由来の不活性濃縮凝固因子製剤を静脈注射することによって、出血症状の予防やコントロールを行います。この濃縮製剤は、多くのドナーによる献血から作られます。
組換えVWFの補充療法
2020年3月に、VWDの新しい治療薬として「ボニコグ アルファ(遺伝子組換え)」(製品名:ボンベンディ)が、国内で承認され、同年5月に保険適用となりました。。ボニコグ アルファは、献血で得られた人間からの血液ではなく、遺伝子組換え技術を使って工業的に作ったVWFです。そのため、献血した人に潜在していた病原体が、製剤に混入するリスクがありません。承認時点で世界初・唯一の遺伝子組換えVWF製剤として、注目されています。
これらの、VWFの値を上げる治療に加え、トラネキサム酸などの線維素溶解阻害剤により出血症状の治療もしくは予防を行ったり、複合経口避妊薬などのホルモン剤で月経過多の治療を行ったりするなど、間接的な止血治療も行われます。
どこで検査や治療が受けられるの?
日本でフォン・ヴィレブランド病の診療を行っていることを公開している、主な施設は以下です。
※このほか、診療している医療機関がございましたら、お問合せフォームからご連絡頂けますと幸いです。
患者会について
※血友病患者さん向けの情報を多く発信されていますが、フォン・ヴィレブランド病患者さん向けの情報も発信されています。
ヘモフィリア友の会全国ネットワークの取材記事は、以下です。








