どのような病気?
「尿素サイクル」とは、主に肝臓で、体内のアンモニア(有毒)を尿素(無毒)に変換する反応で、「オルニチン」「シトルリン」「アルギニノコハク酸」「アルギニン」の4つのアミノ酸を中心に構成されている反応です。
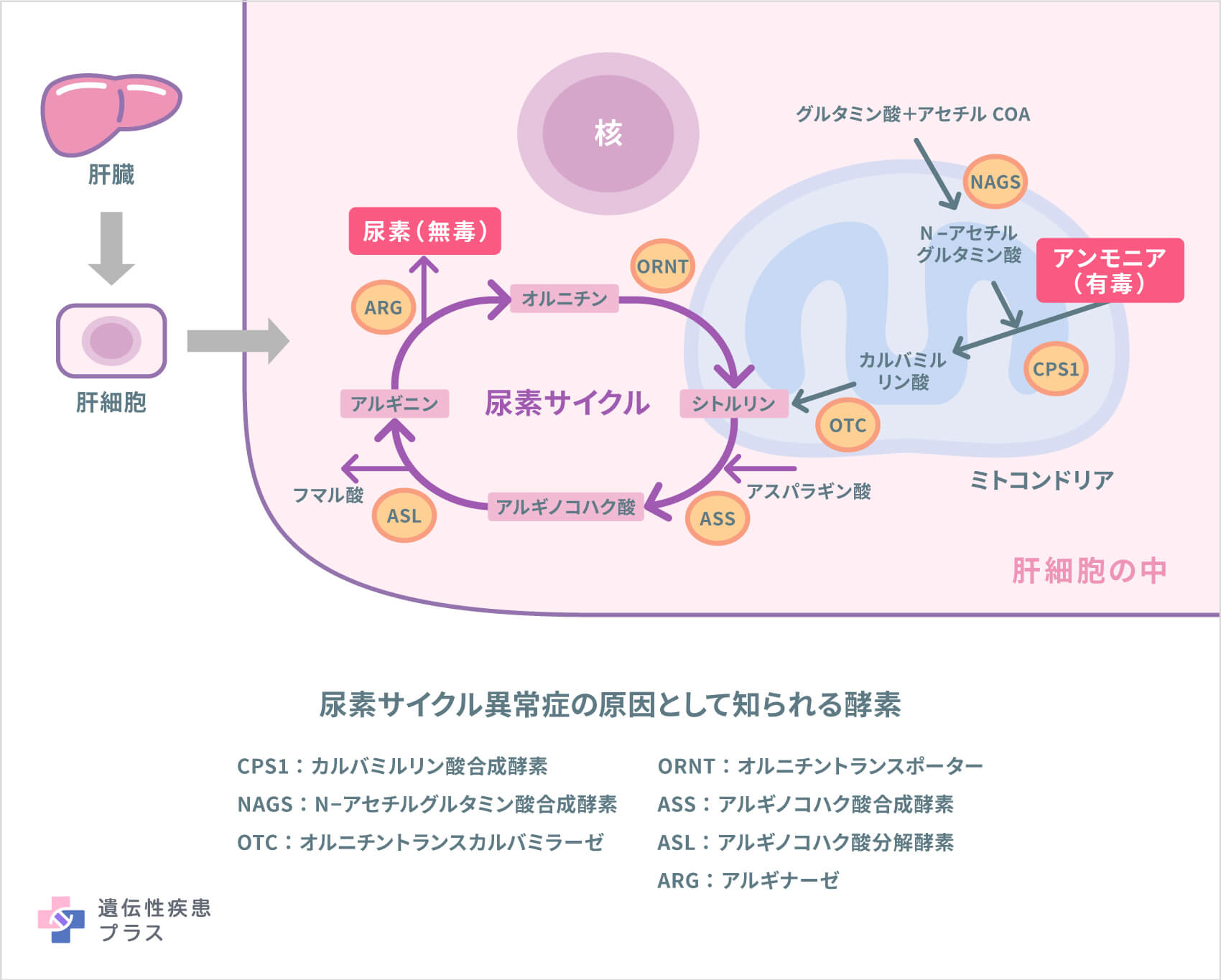
尿素サイクル異常症は、この尿素サイクルに関与する酵素などのタンパク質に異常があることで、高アンモニア血症などを発症する遺伝性疾患をいいます。この病気の原因となるタンパク質は複数あるため、複数の疾患をまとめて「尿素サイクル異常症」と呼びます。
具体的には、「N-アセチルグルタミン酸合成酵素(NAGS)欠損症」「カルバミルリン酸合成酵素(CPS1)欠損症」「オルニチントランスカルバミラーゼ(OTC)欠損症」「急性新生児型シトルリン血症I型」「アルギニノコハク酸尿症」「アルギニン血症」が挙げられ、その他に「高オルニチン高アンモニア血症ホモシトルリン尿症症候群(HHH症候群)」もあります。
これらの疾患は、小児慢性特定疾病の対象疾病となっています。また、HHH症候群は現時点で指定難病となっていませんが、その他は、指定難病対象疾患(指定難病251)となっています。
尿素サイクル異常症による高アンモニア血症でみられる症状は、何となく元気がない、ボーっとする、嘔吐、哺乳力低下、多呼吸、けいれん、意識障害などです。こうした症状に気付いたら、早めに受診し、早期発見を経て早期治療を受けることが重要です。特に発熱したとき、嘔吐したとき、下痢を伴う感染症になったときは、高アンモニア血症を起こしやすいので、注意が必要です。感染症予防のために、予防接種(インフルエンザ、水ぼうそうなど任意接種も含む)は積極的に受けるよう推奨されます。持続する、あるいは繰り返す高アンモニア血症により、中枢神経障害が起こり、発達障害、行動異常、精神障害が生じることがあります。重篤になると、命に関わります。また、乳幼児期の突然死の報告もあります。
症状や重症度は人によって異なり、同じ遺伝子変異をもつきょうだいでも、発症時期や重症度が異なることがあります。女性では、出産後に発症したり、症状の悪化がみられたりする場合もあります。アルギニノコハク酸尿症でよくみられる症状は「髪の毛のねじれ」、アルギニン血症やHHH症候群でよくみられる症状は「小児期から進行する両側まひ」です。これらは、高アンモニア血症がほとんど見られなくても進行します。
尿素サイクル異常症は、8,000人~4万4,000人に1人の割合で発症すると考えられています。日本では、アルギニノコハク酸尿症が7万人に1人、OTC欠損症が8万人に1人、シトルリン血症I型が53万人に1人、CPS1欠損症が80万人に1人、アルギニン血症が220万人に1人との報告があります。長期生存が難しい例も多いため、日本における実際の患者さんの数は、OTC欠損症が約500人、CPSI欠損症が約100人、アルギニノコハク酸尿症が約100人、その他はそれぞれ100人未満と考えられています。
尿素サイクル異常症は、食生活や日常生活が原因で発症することはありません。男女とも発症の可能性がありますが、一部、女性に比べて男性で症状が強いタイプもあります。
家族解析や新生児スクリーニング検査などで、症状が出る前にこの病気が発見される場合もあります。早期に発見され治療を受けた場合、比較的安定に経過することも多いとされています。
こうした早期発見や治療の進歩により、尿素サイクル異常症患者さんの予後は、以前に比べて大きく改善しています。一方で、新生児期発症のOTC欠損症、CPSI欠損症では長期生存が難しい例が少なくありません。男性に比べて軽症の場合が多いOTC欠損症の女性においても、出産後などに急性増悪を発症し、命に関わる場合があります。生命予後や重篤な後遺症は、発症時に最も高くなったときの血中アンモニア値と関連しています。しかし、一時的に著しい高アンモニア血症となっても、速やかに治療を受けて正常値に戻すことで、その後の経過が良好だったという症例もあります。
何の遺伝子が原因となるの?
上述の通り、尿素サイクル異常症は、主に肝臓でアンモニアを無毒な尿素に変換する「尿素サイクル」で働く酵素などのタンパク質の設計図となる遺伝子に異常が起きることで発症します。
それぞれの「疾患(原因遺伝子、染色体位置)」は、「N-アセチルグルタミン酸合成酵素欠損症(NAGS遺伝子、17q21.31)」「カルバミルリン酸合成酵素欠損症(CPS1遺伝子、2q34)」「オルニチントランスカルバミラーゼ欠損症(OTC遺伝子、Xp11.4)」「急性新生児型シトルリン血症I型(ASS1遺伝子、9q34.11)」「アルギニノコハク酸尿症(ASL遺伝子、7q11.21)」「アルギニン血症(ARG1遺伝子、6q23.2)」「高オルニチン高アンモニア血症ホモシトルリン尿症候群(SLC25A15遺伝子、13q14.11)」です。
この病気の、親から子へ遺伝する「遺伝形式」は、原因遺伝子によって異なります。
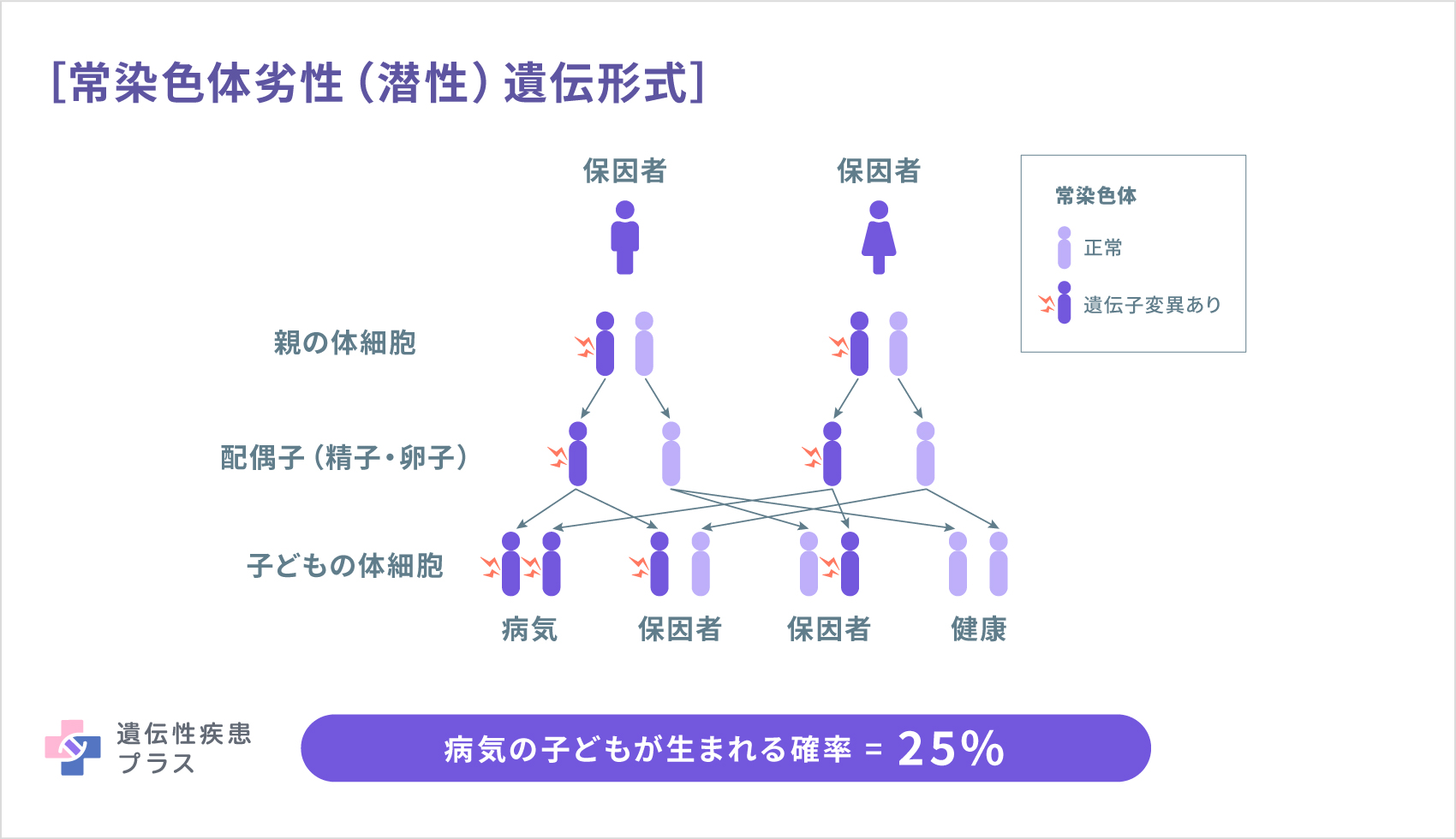
N-アセチルグルタミン酸合成酵素欠損症、カルバミルリン酸合成酵素欠損症、急性新生児型シトルリン血症I型、アルギニノコハク酸尿症、アルギニン血症は、「常染色体劣性(潜性)遺伝」形式で、親から子へ遺伝します。人間が2つ1セットで持っている遺伝子のうち、両親がともに1つずつ変異を有していた場合、子どもは4分の1の確率で2つとも変異を有して、これらの病気を発症します。また、2分の1の確率で1つ変異を有し発症はしない「保因者」となり、4分の1の確率で、発症せず保因者でもなく(変異した遺伝子を持たず)生まれます。
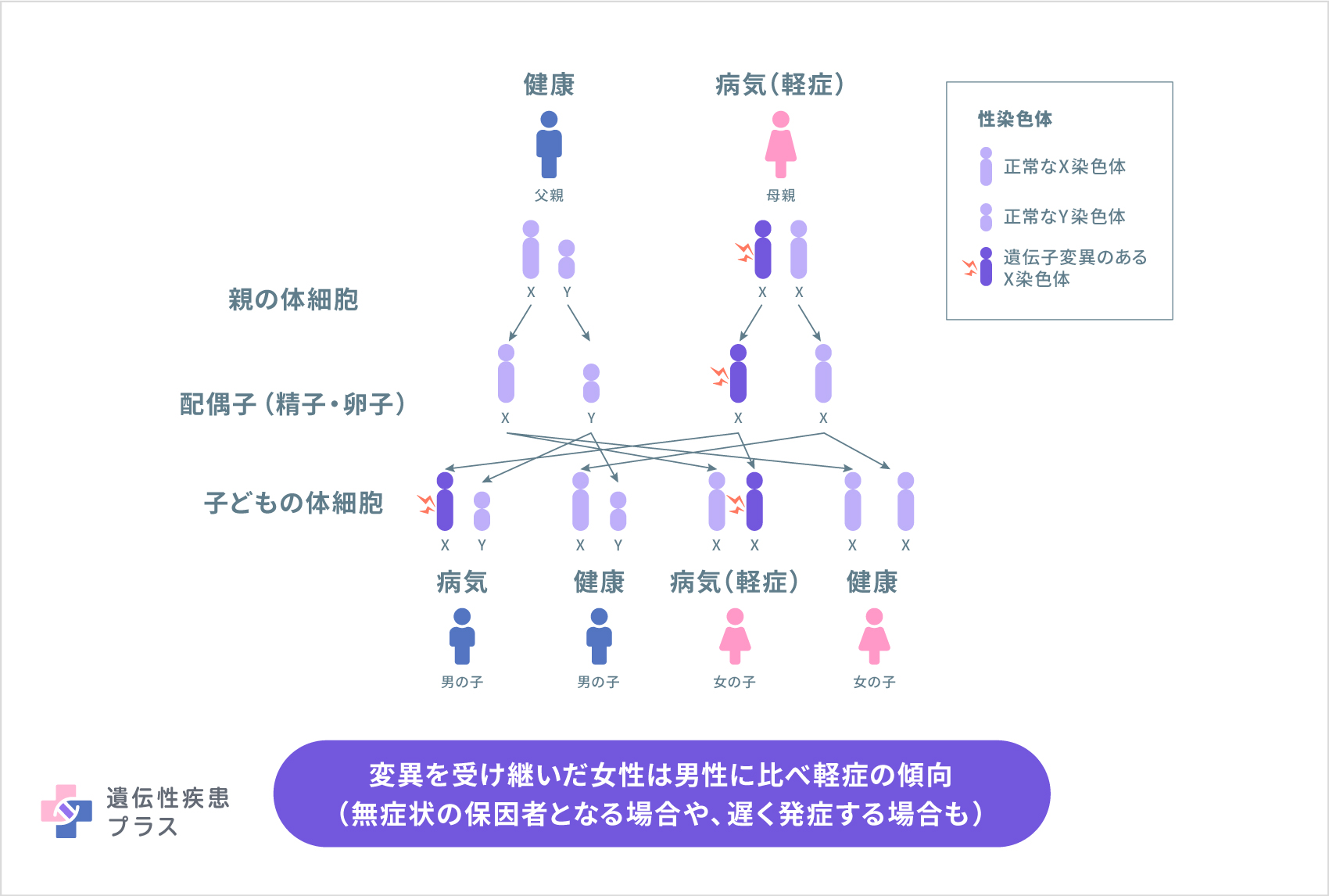
オルニチントランスカルバミラーゼ欠損症は「X連鎖性遺伝(X連鎖性準優性遺伝)」形式で、親から子へ遺伝します。変異した遺伝子を受け継いだ男の子では症状が強く、女の子では男の子より軽症の傾向があり発症年齢にばらつきがあります。その違いには、「X染色体不活化の偏り」という現象が関わっています。女の子は無症状の保因者となる場合や、遅く発症する場合がありますが、発症すると重篤な場合もあります。親には遺伝子変異がなく、子どもで初めて発症する「孤発例」も、少なからずみられます。
どのように診断されるの?
尿素サイクル異常症には、医師が尿素サイクル異常症と診断するための「診断基準」があります。したがって、病院へ行き、必要な問診や検査を受けた後、主治医の先生がそれらの結果を診断基準に照らし合わせ、結果的に尿素サイクル異常症かそうでないかの診断をすることになります。
「嘔気、嘔吐、意識障害、けいれんなどの症状」「3親等内に尿素サイクル異常症の人がいる(オルニチントランスカルバミラーゼ欠損症の場合)」「新生児期にきょうだいが突然死している」のうち1つが当てはまり、さらに「持続的な血中のアンモニア高値:新生児>120µmol/L(200µg/dL)、乳児期以降>60µmol/L(100µg/dL)」を含めて2つ以上が当てはまる場合に、尿素サイクル異常症の疑いとなり、確定診断のための検査が行われます。その他、「アニオンギャップ」という指標が正常(<20)であること、血糖が正常範囲(新生児期>40mg/dL)であることも、検査で確認されます。
確定診断のための検査では、血中や尿中に、この病気に特徴的なアミノ酸などの物質の量の測定や、尿素サイクルではたらく酵素活性の測定、関連する遺伝子の解析などが行われます。
尿素サイクル異常症以外でも、小児期に発症する高アンモニア血症の原因は、その他の先天代謝異常症、先天的脈管形成異常、重症感染症、薬物など、多岐にわたります。そのため、診断の際には、これらの疾患の鑑別が行われます。
どのような治療が行われるの?
尿素サイクル異常症の効果的な治療法は未確立であるため、薬物治療により血中アンモニアの低下を図りつつ、食事療法を行っていきます。治療は、一部の肝移植成功例以外、生涯にわたり受ける必要があります。新生児に対する治療は、専門施設の代謝専門医の協力のもと、チーム体制で行われます。
発症の急性期には、絶食の上、血中アンモニアの低下を図る薬物治療が行われます。薬物療法では、アンモニアを体外に排泄させる薬(安息香酸ナトリウム、フェニル酪酸ナトリウム)が用いられます。これらは、緊急処置時には静脈注射、その後の長期管理時には経口剤として投与されます。また、アルギニンとシトルリンが不足する疾患に対して、アミノ酸療法として、アルギニン(静脈注射)とシトルリン(経口剤)が使用されます。
絶食をすると、エネルギーを取り出すために「タンパク異化」と呼ばれる反応が起こり、その際にアンモニアが出来てしまいます。そのため、こうした急性期の治療では、タンパク異化が起こらないように、十分な量のブドウ糖も投与されます。高血糖の際はインスリンも併用されます。高アンモニア血症の改善が困難であれば、血液透析が行われることもあります。
症状が比較的安定した慢性期では、基本的に食事療法と薬物・アミノ酸療法が行われます。薬物療法やアミノ酸療法は、上述の通りです。食事療法では、栄養障害を起こさないように適切に、タンパク質の量が制限されます。乳児には、特別な調合乳が使用されます。アンモニアのもとになるタンパク質の制限は必要ですが、タンパク質不足になると皮膚炎(おむつかぶれや手足の末端に起きる炎症)、毛髪の脱色、脱毛、脂肪肝が起こります。そのため、その人ごとに、総タンパク質摂取量の目標が決められます。また、タンパク質を制限すると鉄やカルシウム、微量元素の不足、ビタミン不足などにも陥りやすいので、これらの補給が行われます。
治療によるコントロールが難しい場合には、肝移植が行われることもあります。国立成育医療研究センターが行った医師主導治験では、先天性尿素サイクル異常症の赤ちゃんに、生後6日でヒトES細胞由来の肝細胞移植が生後5か月の肝移植までの橋渡し治療として行われ、無事成功しました。現在、安全性や有効性の検証が続けられています。
どこで検査や治療が受けられるの?
日本で尿素サイクル異常症の診療を行っていることを公開している、主な施設は以下です。
- 東北大学病院 小児科
- 埼玉医科大学病院 小児科
- 千葉県こども病院 代謝科
- 日本大学医学部 小児科学系小児科学系分野
- 藤田医科大学医学部小児科学 代謝外来
- 大阪大学大学院医学系研究科 小児科学
- 島根大学医学部附属病院 小児科
※このほか、診療している医療機関がございましたら、お問合せフォームからご連絡頂けますと幸いです。
患者会について
尿素サイクル異常症の患者会で、ホームページを公開しているところは、以下です。
参考サイト
- 難病情報センター
- 小児慢性特定疾病情報センター
- 日本先天代謝異常学会 尿素サイクル異常症の診療ガイドライン
- GRJ 尿素サイクル異常症概説
- 遺伝性疾患プラス ニュース
- NIH Genetics Home Reference








