症状があるのに原因がわからない「未診断疾患」の人たちが適切に診断されるために、2015年に開始した国家プロジェクト、「未診断疾患イニシアチブ(IRUD、アイラッド)」。遺伝性疾患プラスでは2020年に、IRUDについて国立成育医療研究センターゲノム医療研究部部長の要匡(かなめ ただし)先生に詳しくお話を伺い、取材記事として皆さまにお届けしました。その2年後となる2022年4月、IRUDの6年間の成果が公表され、遺伝性疾患プラスでもその内容をニュースとして発信しました。遺伝性疾患プラスの読者の中には実際にIRUDに参加された当事者ご家族なども複数おられ、これまでに編集部にはさまざまなメッセージが寄せられてきています。
そのような中で今回、要先生への取材が再び実現し、IRUDの最新情報をお伺いすることができました。前半では、今回発表された研究の成果や今後の課題などについて詳しくお伺いし、後半では、実際に読者の皆さまから寄せられた質問にお答え頂きました。

IRUDの「いま」と「これから」
まずは2022年4月に国立精神・神経医療研究センターからのプレスリリースとして公表されたIRUDの6年間の成果報告について、より深堀した内容や今後の展望、新たに見えてきた課題など、いろいろお伺いしました。
「2,247家系で657種類の原因遺伝子を特定した」とありますが、この方々の診断がつくまでの平均年数や平均年齢などのデータがあれば教えてください
まずは診断までの平均年数について、今のところはっきりと示せるようなデータはありません。というのは、「いつの時点からを未診断とするのか」を見極めるのが難しいためです。病気の原因がわからない場合、すぐに「あなたは未診断です」ということになるのではなく、多くの場合、原因を見つけるために、さまざまな検査が重ねられていくことになります。そうした病歴は人によってさまざまで、今回のプロジェクトでは、どの時点からが未診断であるとするのかを決めて、個々の患者さんに対して全て記録するような計画にはしていなかったのです。しかし、こうしたデータを取ることも大事だと思うので、今後検討したいと思います。
診断がついた平均年齢については、IRUDは参加時点での年齢の幅が0歳~80歳代までと広いため、これも人それぞれということになるのですが、ざっくりと平均を取ると、7歳くらいになります。IRUD全体の参加者を見るとお子さんが多いため、平均年齢は少ない傾向になります。
前回(2020年)の取材時点では、「IRUDは基本的に全エクソーム解析で行われており、全ゲノム解析に移行しつつある」と伺いましたが、3年経った現在の主な解析手法の状況を教えてください
今も、IRUDは全エクソーム解析をメインとして行っています。これまでプロジェクトを進めてきて、未診断の人の最初のゲノム解析としては、全エクソーム解析を行うのが、解析内容の面でも、費用の面でも、最も効率が良いとわかったからです。報告にあったように、IRUDの6年間の全エクソーム解析で診断がついたのは、参加者の43.8%でした。ここで診断がつかなかった人たちについては現在、主に、政府が実施している「全ゲノム解析等実行計画」により、全ゲノム解析が行われる流れになっています。全ゲノム解析等実行計画は、簡単に言うと、がんや難病(希少遺伝性疾患も含まれる)の患者さん10万人の全ゲノム解析を行い今後の診断精度向上などにつなげる、というものです。このほか、一部の患者さんについては、IRUD自体でも全ゲノム解析を行うことはあります。
2022年3月に、米国のT2Tコンソーシアムにより、ヒトゲノム配列が完全解読されたという発表がありました。この結果は、IRUDにどのようなインパクトを与えていますか?
この結果はIRUDに、直接的に非常に良い影響を与えています。全エクソーム解析などで、病気の原因となっている部分を調べる場合には、特定の病気を発症していない人に共通している「標準ゲノム配列」を参照し、患者さんのゲノム配列と比較する必要があります。今回のT2Tによるヒトゲノムの完全解読によって、より精度の高い標準ゲノム配列が使えるようになりました。具体的には、これまでの標準ゲノム配列では「不明」として一部欠けていた配列が、補填されたイメージです。参照ゲノム配列がより充実したため、これまでのIRUDでは見つけられなかった病気が、新たにいくつか見つけられるようになりました。実際に、IRUDのエクソーム解析で原因が見つからず、全ゲノム解析を行ってもわからず、さらに少し特殊な全ゲノム解析を行い、T2Tの標準ゲノム配列を参照して解析をしたところ、原因がわかったという例もありました。
病気の症状に関連すると考えられる遺伝子にVUSが見つかった場合、その後どのように解析が進められるのでしょうか?
病的意義不明のバリアント(VUS)のうち、病気の原因になっている可能性が考えられるため、もう少し調べる必要があるとなったものについて、モデル生物を用いてその先の解析を行うという新たなプロジェクトが、2017年から、IRUDの成果を進展させる「IRUD Beyond」の一つとして開始されました。プロジェクト名は「J-RDMM」(モデル生物コーディネーティングネットワークプロジェクト)です。このプロジェクトは、カナダで行われている同様のプロジェクト、RDMM(Rare Diseases Models & Mechanisms Network)と情報交換をしながら進めようということになり、頭に日本(Japan)の頭文字を付けたJ-RDMMとして始動しました。
このほか、コンピュータの予測プログラムを用いて、VUSの意義などについての解析が進められています。しかしやはり、モデル動物や細胞を用いて、実際に病気との関連を調べる研究が進められていくことは、メカニズムの解明や、その後の治療法の開発につながる第一歩であり、とても重要なことです。
「難病とゲノムについての医療や研究に関わる非常に多くの人材育成に貢献した」とありますが、具体的な例を教えてください
2020年度までの集計によると、このプロジェクトに関わりながら臨床遺伝専門医を取得した医師が156人、認定遺伝カウンセラー(R)を取得した人は79人でした。実際に未診断疾患や難病の診療に携わったという医師は、のべ人数で4,500人を超えています。ゲノム解析を実際に行うバイオインフォマティシャンも増えました。こうしてIRUDをきっかけに、難病やゲノム医療に携わるようになった人たちが、さらにその先の医療従事者や研究者をIRUDにつなげていき、未診断疾患への関心や、実際に携わる人たちが世の中に広がっていく、といった展開に今後なることを期待しています。
「全国どこにいても誰であっても未診断に苦しむ患者さんが参加できる体制が整った」とありますが、参加に至る明確な「未診断」の定義があれば教えてください
どのような人がIRUDに参加するのか、パンフレット「IRUD(未診断疾患イニシアチブ)のご案内」には次のように書かれています。

参加の条件は幅広く、いろいろなケースが含まれます。「症状があっても原因に基づく診断名がついていない人」が該当するわけなのですが、これは診断する医師側にとっても、判断が難しいところになります。例えば、糖尿病を発症している人がいて、「糖尿病」という病名が付いていても、この糖尿病は、実は他の基となる病気の合併症として発症している場合があります。その、基の病気が見つかっていない場合、未診断疾患として、IRUDの参加条件に当てはまります。通常の糖尿病の治療では改善しなかった患者さんが、IRUDにより原因となる病気が見つかり、その病気の治療を行うことで、糖尿病も改善するというケースも考えられます。ですので、医師が未診断疾患を見極めて、本当の意味での診断につなげることは、非常に重要です。私はこのことを、診療に当たる医師たちに広く理解して頂けるようにと思っており、その一つのアクションとして、先日、日本医師会雑誌に寄稿をしました。
参加できる体制整備により、実際に現在、IRUD参加者は増えているのでしょうか?
IRUDに登録をされる人は、年間約1,000家族(1,000人の患者さんとそのご両親で約3,000人)です。つまり、毎年1,000家族ずつ参加者が増えているということです。一方で、年間のIRUD登録者は、毎年ほとんど変わらず1,000家族程度ずつです。参加への要望は多く頂いていますが、プロジェクト予算との兼ね合いなどで、登録者は同じくらいというのが現状です。
成果と共に見えてきた新たな課題があれば教えてください
一つは、まだまだ認知度が低いことが課題だと思っています。先ほどの、未診断疾患についての理解も含めて、医療者がもっとIRUDを知ることが、未診断疾患を減らしていくために重要です。それとともに、IRUDが「研究」であるということも、正しく理解される必要があります。IRUDは、無料で受けられる単純な検査ではありません。いつも決まった検査だけが行われるというわけではなく、わからない病気の原因を見つけるため、解析方法を工夫したり、結果を見てその先の新たな解析を行ったりするなどして、患者さんと医師が一緒に研究に参加しているという形になります。時間がかかったり、思うようなお知らせが来なかったりすることもあると思いますが、「検査を受けている」というより「研究に参加している」という意識を持っていて頂くと、IRUDのより一層の推進につながるのではないかと思っています。
もう一つ、課題と思っていることは、解析技術の向上です。先ほど、T2Tの標準ゲノム配列が使えるようになり、新たな病気が発見できるようになったとお話ししましたが、それでもまだ診断がつかない人も半数ほどおられます。今後の解析技術の向上で、さらに多くの方の診断がつくようになればと思っています。また、診断がついても、治療法がまだない人も大勢おられます。やはりゴールは、医療として、診断から治療まで患者さんをケアしていくことなので、そのために、病気の原因を見つけるところから治療法を確立するところまで、今後もさまざまな技術の開発が必要だと思っています。
遺伝性疾患プラス読者からの質問
ここからは、実際に読者から遺伝性疾患プラスに寄せられた、IRUDに関する質問について、要先生にお答え頂きました。
子どもがIRUD検査を受けました。検査結果に「今回用いたアレイでは検出が困難な、より狭い領域のコピー数の変化が存在する可能性は否定できません」という一文がありました。これはどういう意味ですか?
専門的な書き方で、難しいですよね。これは、全エクソーム解析の結果ではなく、マイクロアレイ染色体検査という、染色体の小さな構造の変化を調べる検査の結果のように見受けられます。「今回、調べるのに用いたマイクロアレイ検査の解像度では見つけられない、もっと細かい部分に病気の症状に関連するような遺伝子があるかも知れないので、もう少し詳しく調べてみたらわかるかもしれません」、というような意味だと思います。詳しいことは、主治医の先生や、遺伝カウンセリングに関わる方などに質問してみるのが良いでしょう。
「全ゲノム解析ができるようになった」とニュースでは聞くのに、なぜいまだに原因遺伝子が特定できない疾患があるのでしょうか?
ゲノム配列は人によって違う部分があり、これによって一人ひとりの個人差が生じています。実際に個人の全ゲノム解析をすると、標準ゲノム配列と異なる部分は、200万か所以上あります。全エクソーム解析(全ゲノム解析より解析箇所を絞り込んでいる)の場合は、およそ10万か所です。こうした、非常にたくさんの「違っている部分」から、病気と関係している部分を探していくのですが、全ての部分について、「この変化があったらこんな症状が出る」「この変化は症状には関係ない」といったことがわかっているわけではありません。むしろ、大半が、症状との関連性がわからない変化として見つかります。これらについて、ご家族の状態や、コンピュータによる機能予測プログラムなど、いろいろな情報を組み合わせて解析を進め、可能性があるものを徐々に絞り込んでいき、最終的に、病気の原因となっている変化を見つけ出します。
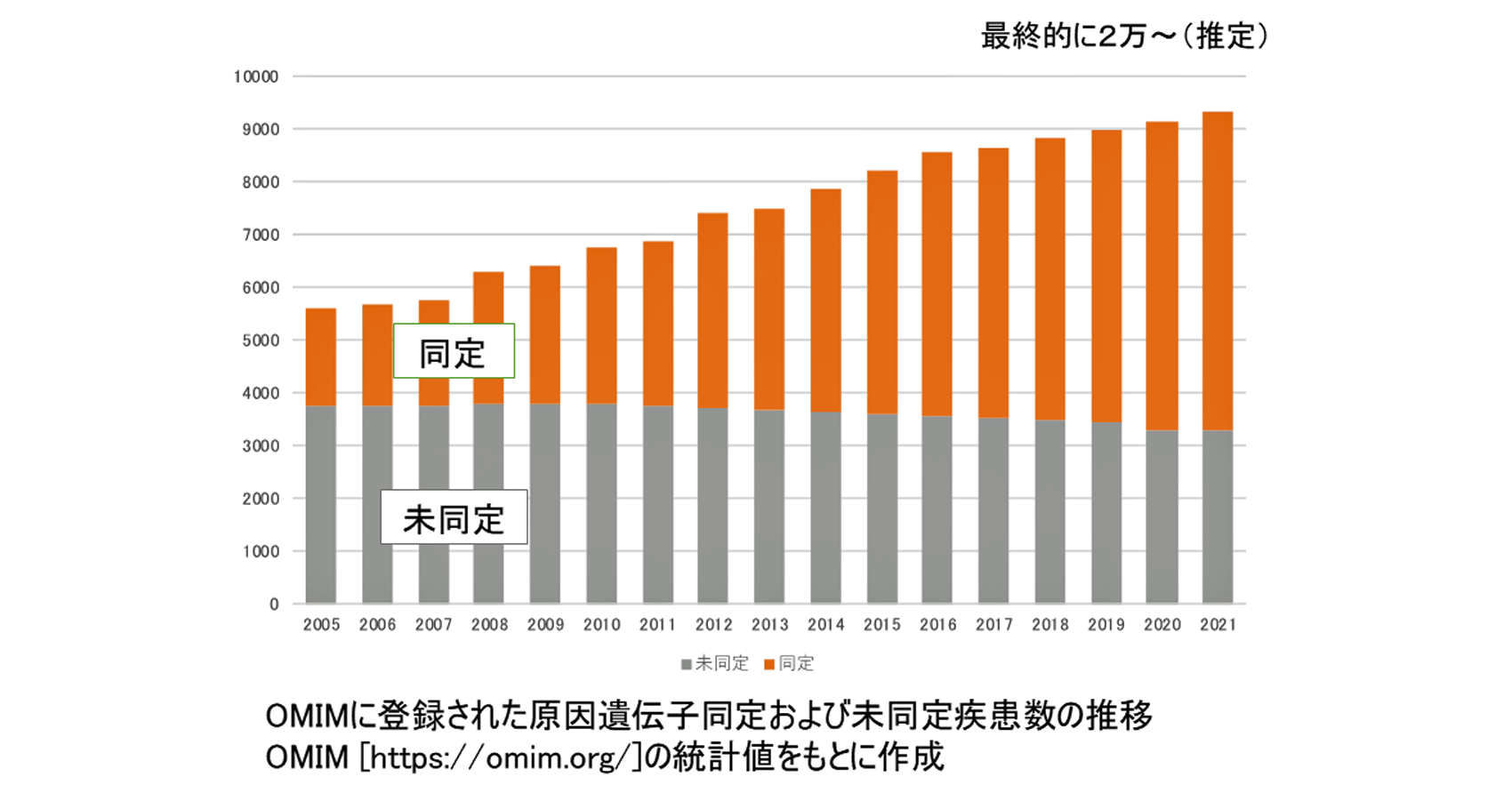
このように、原因遺伝子の特定は、とても大変な作業であるため、まだ全ての希少疾患を見つけ出すには至っていません。一方で、全ゲノム解析ができるようになってから、世界中で新たに見つかる希少遺伝性疾患の数は、年々、確実に増えていっています。遺伝に関連した病気は、「OMIM」という国際的な遺伝性疾患のデータベースに全て登録されていきます。これを見てみると、今、約9,000の希少疾患が見つかっており、そのうち3分の2程度で原因遺伝子が見つかっています。今後の解析の継続と、解析技術の向上により、最終的に希少疾患は2万数千くらい見つかり、その原因遺伝子も特定されていくと予想されています。
IRUDについて、どのくらいの割合の医師が認識し、理解しているのか知りたいです
以前より、確実にIRUDを知っている医師が増えていることは実感しているものの、具体的な統計はまだ取っておらず、今後の調査を検討しているところです。また、IRUDの認知度を上げるために、紹介動画をYouTubeで公開するといった試みも開始しています。
わが子はIRUDに参加し、疾患が確定しました。しかし、IRUDを知っていたわけではなく、また、病院に掲示されているのを見たこともなく、いろいろ調べていく過程で知り、主治医に相談してたどり着きました。なぜ、どこの病院でも幅広くIRUDの存在を知らせてもらえる状況ではないのでしょうか?
私たちも、IRUDをもっと全国的に広く知って頂きたいと思っており、先ほどのYouTubeを公開するなど、努力しています。一方で、IRUDは「研究」なので、ポスターを作ったりCMを流したりするなどの手段で啓発を行う場合にも、研究費として得ている予算の一部を充てることになります。実際、IRUD開始初期にポスターを作って配ったのですが、やはりそれなりの費用がかかってしまいました。「もっとIRUDについて広く知られるべきだ」という、患者さん方の声が国に届き、厚生労働省などが、IRUDのキャンペーンを行って、全国に広めてくれたらありがたいなと思っています。
私の疾患の治療は、現在「対症療法」しかありません。将来、IRUDが進むことで、進行を止める方法がわかったり、新たな治療が開発されたりすることはあるのでしょうか。そうだとすれば、私を含め、希少疾患を持つ人たちへの希望の光になると思います
もちろん、私たちは、病気の原因を見つけたら、最終的に治療法まで確立されることを目標にしています。希少疾患は種類がとても多いため、全てに対してすぐに治療法まで見つけていくというのは難しいところがあります。しかし、研究者も、製薬会社も、こうした希少疾患の進行を止めたり治療したりする方法を見つけることを目指していることは確かです。実際、核酸医薬や、遺伝子治療など、希少遺伝性疾患に対して開発され、使われ始めている治療などもあります。治療法開発に向けてのスピードは、以前より確実に速くなっていると感じています。
遺伝性の希少疾患です。先祖にも同病の人がおそらくいたのではないかと思っています。何世代か前の先祖からも遺伝するような希少疾患はあるのか、あるとしたらその確率はどの程度なのか知りたいです
そういう病気は、あり得ます。実際、家系を調べてみると、遠い親戚にも同じ病気の人がいて、同じ遺伝子の変化でしたという方はおられます。確率は、病気の種類によって違うので、何とも言えません。
検査のため国の施設にサンプルを提供して3年経ちますが、まだ結果が出ずもどかしいです。覚悟はしているので結果を教えて頂きたいのですが、こんなに時間がかかるものなのでしょうか?
かなり待ち遠しいと思います。病気の原因は、見つけやすいものから見つけにくいものまでさまざまで、なかなか見つからないものを調べていくには、どうしても時間がかかってしまいます。とはいえ、参加されている人たちは結果が気になると思われるため、IRUDでは、半年から1年の間に、いったん何らかの結果をお知らせする方針としています。だいぶ待たれて気になっているということで、ぜひ主治医の先生に、「今どういう状況ですか?」と聞いてみて頂ければと思います。
子どもがIRUDで希少遺伝性疾患の診断を受けましたが情報が少なすぎてまだ不安が多いです。国内では初めての診断かもしれないと主治医から言われましたが、世界で何例くらいあるのか、国内に同じ病気の人は他にいないのかなど、情報を入手するにはどのようにしたらよいのでしょうか。同じ病気の仲間がいればつながりたいのです
希少遺伝性疾患ということで、病気の説明をされるときに、臨床遺伝専門医か認定遺伝カウンセラー(R)がおられたと思います。同じ病気の人が世界に何人くらいいるのかなど、これらの人たちに聞いてみるのが一番良いでしょう。先ほどお話ししたOMIMという希少疾患のデータベースで遺伝子を検索すると、世界の患者さんの情報が文献として載っており、臨床遺伝専門医などは、こうした情報を調べて、教えてくれるはずです。
最後に、先生から遺伝性疾患プラスの読者の方々にメッセージをお願い致します
診断がつかないという状態をなくしていくため、IRUDはここまで進んできました。参加された方も、そうでない方も、良かったことも、悪かったことも含め、いろいろ感じていらっしゃると思います。ぜひ、そういったご意見を、主治医の先生などを通して積極的に教えて頂ければと思っています。それを受け、もっと良い体制へと整えていかれればと考えています。
また、IRUDは、やはり研究なので、思い通りにいかないことも、多々あります。しかし、患者さんも医療者も、診断をつけたいという同じ目的でいます。みんなで協力して、日本全体としてもより良い方向に行くように、IRUDを進めていきましょう。
IRUDは、6年間の成果報告後も確実に進展しており、診断がつく人や、新たな希少遺伝性疾患の発見数は、確実に増えているとわかりました。政府が実施する「全ゲノム解析等実行計画」や、遺伝子に見つかった変化が症状に関連しているのかを調べる「J-RDMM」など、新たなプロジェクトの連携も開始していました。一方で、あくまでも研究であるため、思うような結果が得られないことや、IRUD自体の認知度が低いことなど、今後解決すべき課題はまだまだありそうです。こうした課題解決のために、技術開発なども必要ですが、疾患当事者やご家族からの意見なども重要になりそうだとわかりました。
前回、要先生に取材をさせて頂いたときは、新型コロナウイルス対策による自粛が始まった頃で、オンライン取材となりました。あれから3年、自粛も緩和しつつありますが、今回も対面は叶わず、またオンラインとなりました。次こそ、取材の機会が頂けた際には、対面取材が実現すれば良いなと思います。遺伝性疾患プラスは、これからもIRUDの最新情報をお届けしていきます。(遺伝性疾患プラス編集部)







